Việc cấp giấy chứng nhận FDA cho thiết bị y tế là một quy trình quan trọng mà các nhà sản xuất cần thực hiện để đảm bảo rằng sản phẩm của họ đáp ứng các tiêu chuẩn an toàn và hiệu quả của cục quản lý FDA. Thủ tục này không chỉ giúp thiết bị y tế tuân thủ các quy định khắt khe mà còn tăng cường uy tín và khả năng cạnh tranh của doanh nghiệp. Trong bài viết này, Công ty Luật ACC sẽ giới thiệu về Thủ tục cấp Giấy chứng nhận FDA cho thiết bị y tế thông qua bài viết sau.

Thủ tục cấp Giấy chứng nhận FDA cho thiết bị y tế
1. Chứng nhận FDA cho thiết bị y tế là gì?
Chứng nhận FDA cho thiết bị y tế là quy trình mà các thiết bị y tế phải trải qua để được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) phê duyệt trước khi được phép lưu hành và phân phối trên thị trường Hoa Kỳ. Quy trình này nhằm đảm bảo rằng thiết bị y tế đáp ứng các tiêu chuẩn về an toàn, hiệu quả, và chất lượng.
2. Điều kiện cấp giấy chứng nhận FDA cho thiết bị y tế
Để đạt được chứng nhận FDA là điều không đơn giản, đặc biệt sự khác biệt về công nghệ cũng như xã hội giữa Mỹ và Việt Nam khiến cho các doanh nghiệp trong nước ta càng khó khăn hơn. Và dưới đây là một số điều kiện, yêu cầu của Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ mà doanh nghiệp của bạn cần đáp ứng.
- Đăng ký và hồ sơ đầy đủ: Nhà sản xuất phải nộp đơn đăng ký chi tiết, bao gồm mô tả thiết bị, chỉ định sử dụng, quy trình sản xuất, và dữ liệu thử nghiệm. - Hồ sơ phải cung cấp thông tin đầy đủ về thiết bị và chứng minh rằng nó đáp ứng các tiêu chuẩn an toàn và hiệu quả.
- Dữ liệu thử nghiệm và đánh giá: Cung cấp kết quả thử nghiệm lâm sàng hoặc phi lâm sàng chứng minh rằng thiết bị hoạt động hiệu quả và an toàn cho người sử dụng. Các thử nghiệm phải được thực hiện theo các tiêu chuẩn của FDA hoặc các tiêu chuẩn quốc tế chấp nhận được.
- Tuân thủ quy trình sản xuất và kiểm soát chất lượng: Đảm bảo rằng thiết bị được sản xuất theo các thực hành sản xuất tốt (gmp) và quy trình kiểm soát chất lượng. Nhà sản xuất phải có hệ thống kiểm soát chất lượng để đảm bảo thiết bị đáp ứng các tiêu chuẩn an toàn và hiệu quả.
- Cung cấp tài liệu về quy trình và định nghĩa sử dụng: Cung cấp thông tin về quy trình sử dụng thiết bị, hướng dẫn sử dụng, và cảnh báo an toàn. Điều này giúp người sử dụng hiểu rõ cách sử dụng thiết bị một cách an toàn và hiệu quả.
- Chứng minh tính tương đương (nếu cần): Đối với một số thiết bị, chứng minh tính tương đương với một thiết bị đã được phê duyệt trước đó có thể là điều kiện cần thiết. Điều này thường áp dụng cho thiết bị thuộc loại i và loại ii.
Đáp ứng các quy định pháp lý: Tuân thủ các quy định pháp lý và yêu cầu của FDA liên quan đến thiết bị y tế. Điều này bao gồm việc thực hiện các yêu cầu báo cáo và giám sát sau khi thiết bị được phê duyệt.
- Thanh toán phí đăng ký: Thanh toán các khoản phí liên quan đến quy trình cấp giấy chứng nhận FDA. Phí này có thể thay đổi tùy theo loại thiết bị và mức độ phức tạp của hồ sơ.
3. Hồ sơ đăng ký chứng nhận FDA cho thiết bị y tế

Hồ sơ đăng ký chứng nhận FDA
Giấy chứng nhận đăng ký kinh doanh:
- Bản sao giấy chứng nhận đăng ký kinh doanh của doanh nghiệp, xác nhận doanh nghiệp có quyền hoạt động hợp pháp trong quốc gia của mình.
- Thông tin về loại hình kinh doanh, ngành nghề hoạt động, và các chi tiết pháp lý liên quan.
Thông tin về nhà máy sản xuất:
- Địa chỉ cụ thể của nhà máy sản xuất, bao gồm tên đường, số nhà, thành phố, quốc gia.
- Các thông tin chi tiết về nhà máy như diện tích, công suất sản xuất, số lượng nhân viên, và các chứng nhận liên quan đến vệ sinh và an toàn.
Tài liệu kỹ thuật về thiết bị y tế:
- Mô tả chi tiết về thiết bị y tế, bao gồm mục đích sử dụng, cấu tạo, chức năng, và các đặc điểm kỹ thuật.
- Các tài liệu kỹ thuật liên quan, bao gồm bản vẽ kỹ thuật, hướng dẫn sử dụng, và thông số kỹ thuật.
Dữ liệu về quy trình sản xuất:
- Mô tả quy trình sản xuất thiết bị y tế, từ nguyên liệu đầu vào đến sản phẩm hoàn chỉnh.
- Các tài liệu chứng minh việc tuân thủ các quy trình sản xuất và kiểm soát chất lượng.
Kết quả kiểm tra và chứng nhận chất lượng:
- Bản sao giấy chứng nhận chất lượng, chẳng hạn như HCông ty Luật ACCP, ISO 13485 (nếu có), chứng nhận về việc tuân thủ các tiêu chuẩn chất lượng quốc tế.
- Kết quả của các cuộc kiểm tra và đánh giá chất lượng liên quan đến thiết bị y tế.
Thông tin về người liên hệ và đại diện:
- Thông tin liên hệ của người đại diện của doanh nghiệp tại Mỹ, bao gồm địa chỉ, số điện thoại, email.
- Thông tin liên hệ của người chịu trách nhiệm về việc liên lạc với FDA, bao gồm tên, chức vụ, và thông tin liên lạc.
Tài liệu hỗ trợ khác:
- Các báo cáo thử nghiệm và nghiên cứu liên quan đến thiết bị y tế.
- Các tài liệu hỗ trợ khác theo yêu cầu của FDA, như tài liệu về an toàn, hiệu quả, và tuân thủ quy định.
Đơn đăng ký FDA: Đơn đăng ký chứng nhận FDA cho thiết bị y tế, bao gồm các thông tin cần thiết về thiết bị và doanh nghiệp.
4. Trình tự đăng ký chứng nhận FDA cho thiết bị y tế
Bước 1: Tư vấn ban đầu
- Đầu tiên, tổ chức hoặc đơn vị thực hiện dịch vụ chứng nhận FDA sẽ tư vấn cho doanh nghiệp về các quy định, yêu cầu và quy trình cần thiết để đăng ký giấy phép FDA cho thiết bị y tế.
- Doanh nghiệp sẽ được hướng dẫn chi tiết về các hồ sơ, tài liệu và thông tin cần chuẩn bị, bao gồm thông tin về nhà máy sản xuất và tài liệu y tế. Điều này đảm bảo rằng tất cả các thông tin đều chính xác và đầy đủ.
Bước 2: Hướng dẫn kê khai thông tin
- Doanh nghiệp sẽ nhận được hướng dẫn chi tiết về cách kê khai thông tin thiết bị y tế cần thiết cho việc đăng ký FDA.
- Các thông tin cần kê khai bao gồm thông tin doanh nghiệp, thông tin sản phẩm, quy trình sản xuất, chức năng, và các chi tiết kỹ thuật như thông số kỹ thuật.
Bước 3: Tạo tài khoản FDA
- Sau khi thu thập đầy đủ thông tin từ doanh nghiệp, tổ chức thực hiện dịch vụ sẽ tiến hành tạo tài khoản cho doanh nghiệp trên hệ thống FDA.
- Việc tạo tài khoản này là bước đầu tiên để kết nối doanh nghiệp với hệ thống quản lý của FDA.
Bước 4: Đăng nhập và kê khai chi tiết
- Tổ chức thực hiện dịch vụ sẽ đăng nhập vào hệ thống FDA bằng tài khoản đã tạo, sau đó tiến hành đăng ký và kê khai chi tiết về sản phẩm của doanh nghiệp.
- Các chi tiết kê khai bao gồm mô tả sản phẩm, thành phần, quy trình sản xuất và các thông số kỹ thuật cần thiết.
Bước 5: Cập nhật mã PIN và mã PCN
- Sau khi nhận được phí đăng ký từ doanh nghiệp, hệ thống FDA sẽ tự động cập nhật mã PIN (Personal Identification Number) và mã PCN (Product Code Number) vào tài khoản đã đăng ký của doanh nghiệp.
- Các mã này rất cần thiết để tiếp tục quá trình đăng ký và xác nhận sản phẩm.
Bước 6: Nhập mã và nộp hồ sơ
- Khi đã nhận được mã PIN và mã PCN, tổ chức chứng nhận sẽ nhập các mã này vào hệ thống FDA.
- Sau đó, tổ chức sẽ nộp hồ sơ đăng ký và hệ thống sẽ cấp số FDA tạm thời cho doanh nghiệp.
Bước 7: Bàn giao giấy chứng nhận tạm thời
- Tổ chức chứng nhận sẽ bàn giao giấy chứng nhận mã số FDA tạm thời đã được xác thực cho doanh nghiệp.
- Giấy chứng nhận tạm thời này cho phép doanh nghiệp bắt đầu kinh doanh và phân phối sản phẩm trong khi chờ đợi giấy chứng nhận chính thức từ FDA.
Bước 8: Bàn giao giấy chứng nhận chính thức
- Sau khi hồ sơ được FDA đánh giá và phê duyệt hoàn toàn, doanh nghiệp sẽ nhận được giấy chứng nhận FDA chính thức cho thiết bị y tế.
- Giấy chứng nhận này xác nhận rằng thiết bị y tế của doanh nghiệp đã đáp ứng đầy đủ các tiêu chuẩn và quy định của FDA.
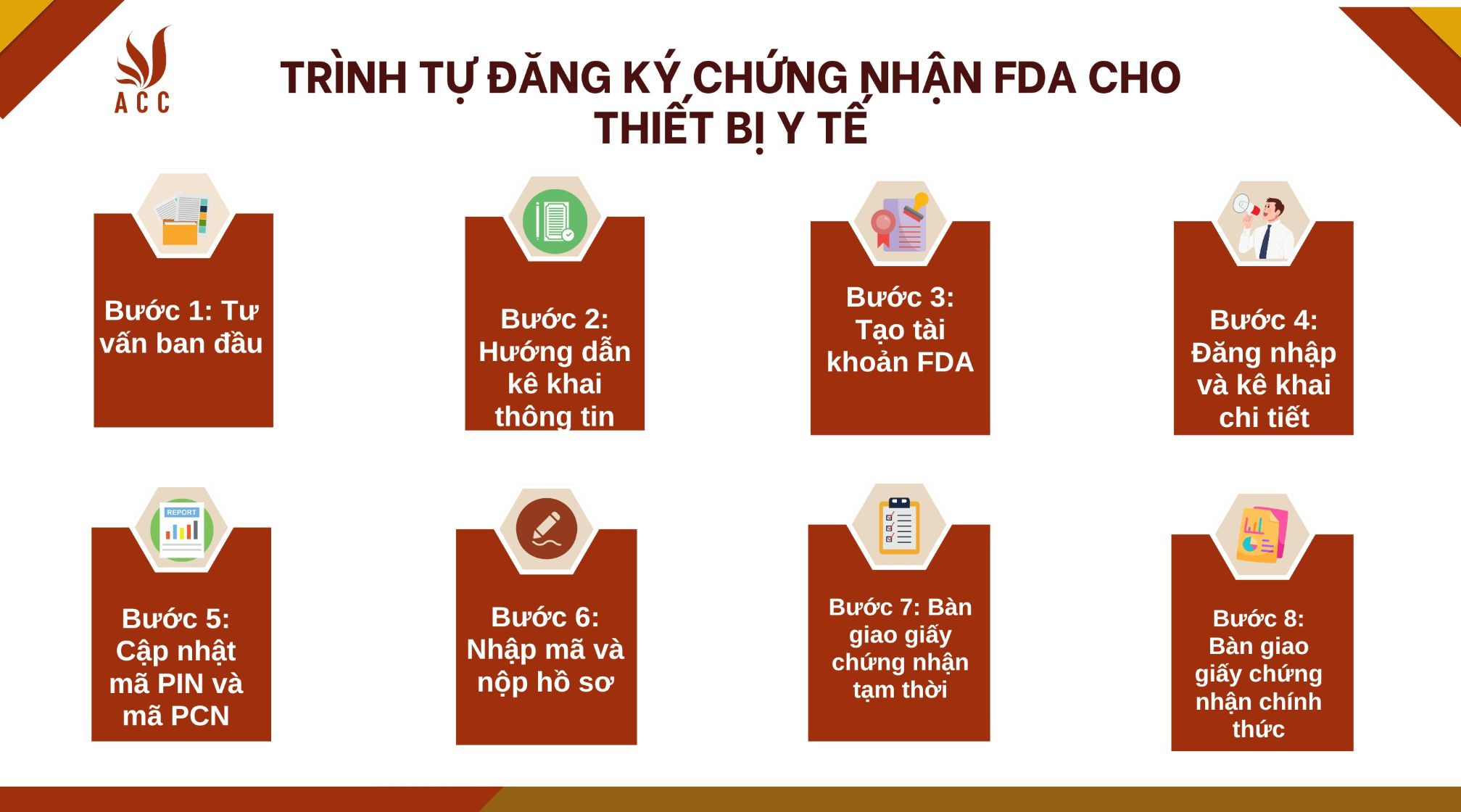
Trình tự đăng ký chứng nhận FDA cho thiết bị y tế
5. Cách phân loại thiết bị y tế theo FDA
5.1. Lớp I
Đặc điểm
- Là những thiết bị y tế phổ biến, được sử dụng hàng ngày.
- Có nguy cơ gây hại thấp hoặc không có rủi ro đối với người dùng.
- Các sản phẩm trong nhóm này không được sử dụng để hỗ trợ, duy trì sự sống, hoặc có tầm quan trọng đáng kể trong việc cải thiện sức khỏe của người dùng.
Điều kiện được tung ra thị trường
- Không cần đăng ký Premarket Notification (PMN) hoặc Premarket Approval (PMA).
- Chịu sự kiểm soát chung.
- Phải tuân theo chính sách và quy định của FDA về việc đăng ký thiết bị y tế.
- Tuân thủ nhãn hiệu và chất lượng sản phẩm phù hợp.
- Thông báo cho FDA trước khi bán sản phẩm.
Ví dụ: Băng thun, găng tay, mũ phẫu thuật, dây đeo vai y tế, xe lăn, bàn chải, chỉ nha khoa, máy trợ thính, khăn trải giường, chất bôi trơn...
5.2. Lớp II
Đặc điểm
- Được coi là những thiết bị rủi ro trung bình.
- Tiếp xúc với cơ quan và hệ thống nội tạng của bệnh nhân.
- Có tác động nhiều hơn đến sức khỏe tổng thể của bệnh nhân.
Điều kiện được tung ra thị trường
- Tuân thủ theo chính sách và quy định của FDA về việc đăng ký thiết bị y tế.
- Chịu sự kiểm soát đặc biệt.
- Phải tuân theo quy trình nộp và xem xét thông báo trước khi sản phẩm ra thị trường của FDA (PMN).
Ví dụ: Máy X-quang, kim châm cứu, máy sưởi ấm sơ sinh, ống thông, máy đo huyết áp, ống tiêm, xe lăn chạy bằng điện, bộ dụng cụ truyền máu, máy bơm sữa, máy đo điện tâm đồ, hệ thống theo dõi sức khỏe...
5.3. Lớp III
Đặc điểm
- Các thiết bị trong lớp này có độ rủi ro cao.
- Thường là sản phẩm hỗ trợ và duy trì sự sống của con người.
Điều kiện được tung ra thị trường
- Chịu sự kiểm soát chung.
- Tuân thủ quy định nghiêm ngặt.
- Phải tuân theo hướng dẫn của lớp I và II.
- Phải trải qua quy trình Premarket Approval (PMA) của FDA.
Ví dụ: máy tạo nhịp tim cấy ghép, máy tạo xung, máy thở, xét nghiệm chẩn đoán HIV, tia laser chữa trị, vòng tránh thai, hệ thống ốc tai điện tử, máy theo dõi sức khỏe thai nhi, các bộ phận giả được cấy ghép…
Để biết thêm về Thủ tục xin cấp giấy chứng nhận FDA Hoa Kỳ tại Việt Nam vui lòng tham khảo tại đây!
6. Câu hỏi thường gặp
Quy trình phê duyệt FDA cho thiết bị y tế mất bao lâu?
Câu trả lời: Quy trình phê duyệt FDA cho thiết bị y tế thường mất từ 3 đến 6 tháng. Thời gian này có thể thay đổi tùy thuộc vào mức độ phức tạp của thiết bị và sự đầy đủ của hồ sơ đăng ký. Nếu FDA yêu cầu thêm thông tin hoặc tài liệu bổ sung, thời gian xử lý có thể kéo dài.
Có những loại thiết bị y tế nào không cần phải xin cấp giấy chứng nhận FDA?
Câu trả lời: Một số loại thiết bị y tế không cần phải xin cấp giấy chứng nhận FDA, bao gồm:
- Thiết bị thuộc loại III: Thường yêu cầu quy trình phê duyệt nghiêm ngặt hơn gọi là PMA (premarket approval).
- Thiết bị đã được phân phối trước ngày 28/05/1976: Và không có thay đổi đáng kể về mẫu mã, thành phần, quy trình sản xuất hay mục đích sử dụng.
- Thiết bị không được tiếp thị thương mại: Hoặc chỉ sử dụng trong nghiên cứu.
Tôi có thể theo dõi tiến trình hồ sơ đăng ký FDA của mình như thế nào?
Câu trả lời: Bạn có thể theo dõi tiến trình hồ sơ đăng ký FDA của mình thông qua hệ thống điện tử FDA. Hệ thống này cung cấp thông tin cập nhật về tình trạng hồ sơ, bao gồm các bước đã hoàn tất và yêu cầu bổ sung. Bạn cũng có thể liên hệ trực tiếp với FDA để yêu cầu thông tin về tiến trình hồ sơ.
Trên đây là một số thông tin chi tiết về Thủ tục cấp Giấy chứng nhận FDA cho thiết bị y tế. Hy vọng với những thông tin Công ty Luật ACC đã cung cấp sẽ giúp bạn hiểu thêm về vấn đề trên. Nếu bạn cần hỗ trợ tư vấn pháp lý hoặc sử dụng các dịch vụ pháp lý khác từ chúng tôi, hãy đừng ngần ngại mà liên hệ với chúng tôi để được hỗ trợ nhanh chóng. Chúng tôi cam kết sẽ giúp bạn có trải nghiệm tốt nhất về các dịch vụ mà mình cung cấp đến khách hàng. Chúng tôi luôn đồng hành pháp lý cùng bạn.
Nội dung bài viết:






Bình luận